Tai-Nagara, I.., et al. (2020) Blood and lymphatic systems are segregated by the FLCN tumor suppressor. Nature Communications. doi.org/10.1038/s41467-020-20156-6
研究者评论:
这些结果具有重要的学术意义,因为它们阐明了一个多年来一直没有答案的生物学问题:为什么体内两个非常相似的循环系统——血管和淋巴管,会形成并维持独立的网络?从临床的角度来看,这有可能为癌症转移的机制提供线索,并有可能发展成为治疗淋巴水肿的新方法。
在癌症手术中,由于引流淋巴液的能力下降,淋巴结切除会导致上肢和下肢严重水肿。物理疗法、弹力袜和淋巴静脉吻合术被列为治疗方法,但即使有熟练的显微手术技术,也难以保证理想的治疗效果。在这项研究中,我们设想了一种未来创新的淋巴水肿治疗方法,我们可以通过药物干预 FLCN 的信号通路,以人工创建局部连接静脉和淋巴管的分流。”
Masaya Baba ,熊本大学副教授
日本熊本大学的研究人员阐明了血管和淋巴管在发育后保持相互隔离的机制。这两种循环系统管路的特征和结构非常相似,关于它们如何保持相互分离,多年来一直无法解释。在这项研究中,研究人员发现血管内皮细胞中的分子滤泡蛋白 (FLCN) 充当了维持这种隔离的守门人。
血液和淋巴管形成独立的网络,直到颈部左右静脉角最终汇合。血管充当将氧气从肺部输送到全身组织的管道。另一方面,淋巴管吸收不能被血管收集的组织液,并作为免疫系统的一部分。然而,血管和淋巴管的特征和结构非常相似,因此它们如何保持相互分离一直是个谜。
阐明这一机制可为开发治疗人类淋巴疾病的新方法奠定基础。例如,创建允许以往阻塞的淋巴流直接返回静脉的旁路(静脉淋巴分流)将成为术后淋巴水肿的创新疗法。因此,世界各地的研究人员一直在研究血液淋巴管分离机制,但仍未完全了解。
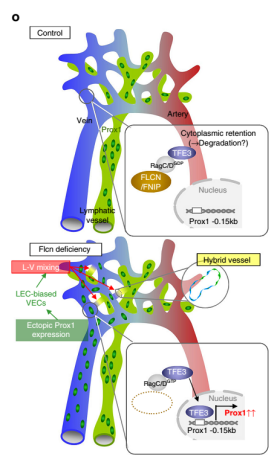

在这项研究中,研究人员首先关注FLCN,这是一种遗传性疾病的致病基因,具有多发性肺囊肿、肾癌和良性皮肤肿瘤(Birt-Hogg-Dube 综合征)的典型症状。他们发现,在血管内皮细胞中缺失Flcn基因的小鼠在血管和淋巴管之间存在异常吻合,导致胎儿死亡。此外,即使在具有正常血液和淋巴管分离的新生小鼠中,内皮细胞中诱导的Flcn基因缺失也会导致两种血管类型之间的异常吻合。
Flcn缺乏会产生偏向淋巴管的血管内皮细胞。这些细胞导致血管和淋巴管之间的吻合。Prox1 是调节淋巴管生成的中心转录因子,其表达被静脉内皮细胞中的 Flcn 抑制,以维持血管内皮细胞的特性。
然而,当血管内皮细胞中的 Flcn 调节丧失时,Prox1 会表达,使静脉内皮细胞偏向淋巴管结构。研究人员还发现,Flcn的缺失会导致通常位于细胞质中的转录因子 Tfe3 易位到细胞核中,从而直接上调 Prox1 的表达。事实上,当Flcn敲除小鼠与Tfe3敲除小鼠杂交时,在没有Tfe3和Flcn的情况下,Prox1 不表达,并且未观察到淋巴偏向的静脉内皮细胞。这些结果表明,FLCN 充当了调节可塑性并保持血液和淋巴管分离的看门人。