Scallan, J.P., et al. (2021) Foxo1 deletion promotes the growth of new lymphatic valves. Journal of Clinical Investigation. doi.org/10.1172/JCI142341
Florida大学(USF Health)的一项临床前研究获得了出人意料的成果,Foxo1基因被确定为遗传性淋巴水肿的潜在治疗靶点。这项由杜兰大学(Tulane)和密苏里大学Missouri的研究者共同得出的结果于 2021年7 月15 日发表在《 The Journal of Clinical Investigation》上。
淋巴水肿 -原发性或遗传性淋巴水肿比较少见,通常出生时就会发病,部分原因是由于关系到淋巴瓣膜正常发育的基因突变引起的。继发性淋巴水肿是由手术、放射治疗、外伤或寄生虫感染对淋巴系统造成的损害引起的。在美国,淋巴水肿最常影响乳腺癌患者,在淋巴结切除和放射治疗后患病率从 10% 到 40% 不等。
虽然淋巴水肿可以通过手法引流(MLD)和压力治疗(CT)来控制,但这些治疗方法无法解决根本原因:液体最终会在淋巴系统中积聚,就像排水管堵塞后溢出水槽一样,这种停滞的淋巴通路会引发炎症反应,导致结缔组织和脂肪组织形成并硬化皮肤,限制运动能力并增加复发性感染的风险。
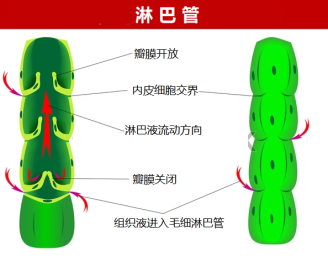

淋巴管内有单向开关的瓣膜,在淋巴循环中起到重要的作用,瓣膜缺失或功能障碍与淋巴水肿的发病密切相关。但是,过去未发现生成新的瓣膜,或者修复有缺陷的瓣膜的方法或机制,而此次USF Health的研究表明,以上两者都是可能的。
根据 USF Health 此前发现的控制淋巴瓣膜形成的细胞信号传导过程,研究小组推导Foxo1基因编码的蛋白质在淋巴瓣膜形成中起关键作用。研究人员表明,与没有Foxo1缺失的对照同源小鼠相比,消除单个基因-淋巴管特异性Foxo1 - 在年轻的产后小鼠和成年小鼠中显著促进了更多瓣膜的生长。此外,在模拟人类淋巴水肿的小鼠模型中消除Foxo1可以完全恢复瓣膜数量和功能。
“令人兴奋的是,Foxo1是迄今为止报道的唯一一个淋巴水肿相关基因,当它被消除时,会诱导生成更多的淋巴瓣膜,而不是抑制瓣膜生长,”研究者表示:“我们实际上在淋巴水肿的基因突变模型中逆转了瓣膜缺失并修复了有缺陷的瓣膜的结构和功能……这个发现赋予研究以非凡的临床意义。”
淋巴循环系统与血管循环系统共通——通过收集和控制从组织中渗出的淋巴液的流动,帮助维持体内健康的体液平衡。这个复杂的网络将携带蛋白质、营养物质和免疫细胞的淋巴液沿一个方向流经全身,然后将液体返回到循环系统的血液中。淋巴管内的瓣膜根据淋巴液运行需要打开和关闭,使其向前移动并防止回流到组织中。
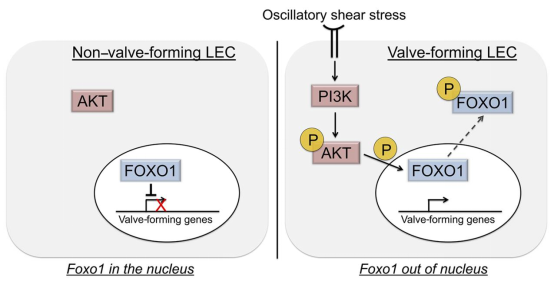

主要研究结果包括:
1.蛋白质 FOXO1(由Foxo1基因编码)通过影响许多基因来抑制淋巴瓣膜的发育,这些基因共同促成了制造成熟瓣膜的多个步骤的过程。FOXO1 的行为就像一组瓣膜形成基因的制动器。“一旦刹车被移除,所有这些基因现在都可以表达出来,这样新的瓣膜就可以成功生长。”
2.Foxo1在年轻产后小鼠淋巴管内皮细胞 (LEC) 中的失活(敲除)促进了多个阶段的瓣膜形成。同样,与没有基因敲除的对照小鼠相比,在成年小鼠中删除 LEC 特异性Foxo1也会增加瓣膜的形成。
3.淋巴水肿小鼠模型的淋巴瓣膜减少了 50%,其余瓣膜异常关闭并表现出液体返流。当Foxo1被消除时,瓣膜的数量增加到与健康对照小鼠相同的水平,并且有缺陷的瓣膜结构恢复正常。进一步分析表明,在这种人类原发性淋巴水肿疾病小鼠模型中, Foxo1的缺失也显著改善了瓣膜功能。